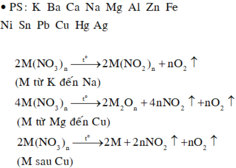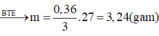nhiệt phân hoàn toàn m gam hh X gồm Pb(no3)2 và Agno3 thu được 12.32 lít hh khí Y.sau khi làm lạnh hỗn hợp Y để hóa lỏng no2 thì còn lại 1 khí với thể tích 3.36 lit.tính tp % số mol của muối chì trong hh.(đktc)
2Pb(NO3)2 ------t*---> 4NO2 + O2 + 2PbO
a________________2a____a/2
2AgNO3 ----------t*---> 2Ag + 2NO2 + O2
b________________b_____b_____b/2
sau phản ứng thu đc hỗn hợp khí O2 và NO2 :
--> 2a + a/2 + b + b/2 = 12,32/22,4 = 0,55 mol ---> 5a/2 + 3b/2 = 0,55 mol (1)
hóa lỏng NO2 khí còn lại là : O2 = 3,36 lýt
---> a /2 + b/2 = 0,15 mol ----> a + b = 0,3 mol (2)
giải hệ (1) và (2) -----> a = 0,1 . b = 0,2
--> m Pb(NO3)2 = 0,1 x 331 = 33,1 g
mAgNO3 = 0,2 x 170 = 34 g
---> % m Pb(NO3)2 = 33,1/(33.1 + 34) = 49,33 %
---> % mAgNO3 = 100 - 49,33 = 50,67 %
Đúng 0
Bình luận (1)
Nhiệt phân hoàn toàn m gam hỗn hợp X gồm Pb(NO3)2 và AgNO3 thu được 12,32 lít hỗn hợp khí Y. Sau khi làm lạnh hỗn hợp Y để hoá lỏng NO2 thì còn lại một khí với thể tích là 3,36 lít. Tính thành phần % khối lượng các muối có trong hỗn hợp X. Biết thể tích các khí được đo ở đktc.A.35,3% và 64,7% B.65,5% và 34,5%C.49,7% và 50,3 % D.50,3 % và 64,7%
Đọc tiếp
Nhiệt phân hoàn toàn m gam hỗn hợp X gồm Pb(NO3)2 và AgNO3 thu được 12,32 lít hỗn hợp khí Y. Sau khi làm lạnh hỗn hợp Y để hoá lỏng NO2 thì còn lại một khí với thể tích là 3,36 lít. Tính thành phần % khối lượng các muối có trong hỗn hợp X. Biết thể tích các khí được đo ở đktc.
A.35,3% và 64,7%
B.65,5% và 34,5%
C.49,7% và 50,3 %
D.50,3 % và 64,7%
Pb(NO3)2 = PbO + 2NO2 + ½ O2
AgNO3 = Ag + NO2 + ½ O2
nO2 = 0,15 mol. nNO2 = 0,4 mol
giải hệ phương trình ta đc, nAgNO3 = 0,2 mol, n Pb(NO3)2 = 0,1 mol
% Pb(NO3)2 = 49,65%
Đúng 0
Bình luận (0)
Nhiệt phân hoàn toàn 20,2 gam hỗn hợp gồm Cu(NO3)2 và Fe(NO3)2 thu được hỗn hợp khí X. Dẫn từ từ hỗn hợp khí X vào nước (không có không khí), sau khi các phản ứng xảy ra hoàn toàn thu được 2 lít dung dịch Y và còn 0,448 lít khí (đktc) thoát ra. pH của dung dịch Y là A. 1,3. B. 2. C. 1. D. 2,3.
Đọc tiếp
Nhiệt phân hoàn toàn 20,2 gam hỗn hợp gồm Cu(NO3)2 và Fe(NO3)2 thu được hỗn hợp khí X. Dẫn từ từ hỗn hợp khí X vào nước (không có không khí), sau khi các phản ứng xảy ra hoàn toàn thu được 2 lít dung dịch Y và còn 0,448 lít khí (đktc) thoát ra. pH của dung dịch Y là
A. 1,3.
B. 2.
C. 1.
D. 2,3.
Đáp án C
2Cu(NO3)2 → t ° 2CuO + 4NO2↑+ O2↑ (1)
2x →4x → x (mol)
4Fe(NO3)2 → t ° 2Fe2O3 + 8NO2↑ + O2↑ (2)
4y → 8y → y (mol)
4NO2 + O2 + 2H2O → 4HNO3 (3)
Ta thấy ở PTHH (1) và (3): nNO2: nO2 = 4: 1
ở PTHH (2) nNO2 : nO2 = 8 : 1
=> số khí thoát ra chính là khí NO2 dư ở PTHH (2)
=> nNO2 = 0,448 : 22,4 = 0,02 (mol)
=> 4y = 0,02 => y = 0,005 (mol)
BTKL: mhh = 188.2x + 180.4y = 20,2
=> x= 0,044 (mol)
=> nHNO3 = 2nCu(NO3)2 + 2nFe(NO3)2 – nNO2 dư = 2. 2.0,044 + 2. 4.0,005 – 0,02 = 0,196 (mol)
=> CM HNO3 = 0,196 : 2 = 0,098 (M)
=> pH = -log [HNO3] = 1
Đúng 0
Bình luận (0)
Nhiệt phân hoàn toàn 20,2 gam hỗn hợp gồm Cu(NO3)2 và Fe(NO3)2 thu được hỗn hợp khí X. Dẫn từ từ hỗn hợp khí X vào nước (không có không khí), sau khi các phản ứng xảy ra hoàn toàn thu được 2 lít dung dịch Y và còn 0,448 lít khí (đktc) thoát ra. pH của dung dịch Y là A. 1,3. B. 2. C. 1. D. 2,3.
Đọc tiếp
Nhiệt phân hoàn toàn 20,2 gam hỗn hợp gồm Cu(NO3)2 và Fe(NO3)2 thu được hỗn hợp khí X. Dẫn từ từ hỗn hợp khí X vào nước (không có không khí), sau khi các phản ứng xảy ra hoàn toàn thu được 2 lít dung dịch Y và còn 0,448 lít khí (đktc) thoát ra. pH của dung dịch Y là
A. 1,3.
B. 2.
C. 1.
D. 2,3.
2Cu(NO3)2 2CuO + 4NO2↑+ O2↑ (1)
2x →4x → x (mol)
4Fe(NO3)2 2Fe2O3 + 8NO2↑ + O2↑ (2)
4y → 8y → y (mol)
4NO2 + O2 + 2H2O → 4HNO3 (3)
Ta thấy ở PTHH (1) và (3): nNO2: nO2 = 4: 1
ở PTHH (2) nNO2 : nO2 = 8 : 1
=> số khí thoát ra chính là khí NO2 dư ở PTHH (2)
=> nNO2 = 0,448 : 22,4 = 0,02 (mol)
=> 4y = 0,02 => y = 0,005 (mol)
BTKL: mhh = 188.2x + 180.4y = 20,2
=> x= 0,044 (mol)
=> nHNO3 = 2nCu(NO3)2 + 2nFe(NO3)2 – nNO2 dư = 2. 2.0,044 + 2. 4.0,005 – 0,02 = 0,196 (mol)
=> CM HNO3 = 0,196 : 2 = 0,098 (M)
=> pH = -log [HNO3] = 1
Đáp án C
Đúng 1
Bình luận (0)
Nhiệt phân hoàn toàn 20,2 gam hỗn hợp gồm Cu(NO3)2 và Fe(NO3)2 thu được hỗn hợp khí X. Dẫn từ từ hỗn hợp khí X vào nước (không có không khí), sau khi các phản ứng xảy ra hoàn toàn thu được 2 lít dung dịch Y và còn 0,448 lít khí (đktc) thoát ra. pH của dung dịch Y là A. 1,3 B. 2. C. 1. D. 2,3
Đọc tiếp
Nhiệt phân hoàn toàn 20,2 gam hỗn hợp gồm Cu(NO3)2 và Fe(NO3)2 thu được hỗn hợp khí X. Dẫn từ từ hỗn hợp khí X vào nước (không có không khí), sau khi các phản ứng xảy ra hoàn toàn thu được 2 lít dung dịch Y và còn 0,448 lít khí (đktc) thoát ra. pH của dung dịch Y là
A. 1,3
B. 2.
C. 1.
D. 2,3
Chọn C
2Cu(NO3)2 → t ° 2CuO + 4NO2↑+ O2↑ (1)
2x →4x → x (mol)
4Fe(NO3)2 → t ° 2Fe2O3 + 8NO2↑ + O2↑ (2)
4y → 8y → y (mol)
4NO2 + O2 + 2H2O → 4HNO3 (3)
Ta thấy ở PTHH (1) và (3): nNO2: nO2 = 4: 1
ở PTHH (2) nNO2 : nO2 = 8 : 1
=> số khí thoát ra chính là khí NO2 dư ở PTHH (2)
=> nNO2 = 0,448 : 22,4 = 0,02 (mol)
=> 4y = 0,02 => y = 0,005 (mol)
BTKL: mhh = 188.2x + 180.4y = 20,2
=> x= 0,044 (mol)
=> nHNO3 = 2nCu(NO3)2 + 2nFe(NO3)2 – nNO2 dư = 2. 2.0,044 + 2. 4.0,005 – 0,02 = 0,196 (mol)
=> CM HNO3 = 0,196 : 2 = 0,098 (M)
=> pH = -log [HNO3] = 1
Đúng 0
Bình luận (0)
nung m gam hỗn hợp X gồm Zn(NO3)2 và NaNO3 ở nhiệt độ cao đến phản ứng hoàn toàn thu được 8.96 lít hỗn hợp khí Y(đktc). cho khí hấp thụ vào nước thu được 2 lít dung dịch Z và còn lại thoát ra 3,36 lít khí .tính pH của dung dịch Z
Nung m gam hỗn hợp X gồm Zn(NO3)2 và NaNO3 ở nhiệt độ cao đến phản ứng hoàn toàn, thu được 8,96 lít hỗn hợp khí Y (đktc). Cho khí hấp thụ vào nước thu được 2 lít dung dịch Z và còn lại thoát ra 3,36 lít khí (đktc). pH của dung dịch Z là A. pH 0. B. pH 1. C. pH 2. D. pH 3.
Đọc tiếp
Nung m gam hỗn hợp X gồm Zn(NO3)2 và NaNO3 ở nhiệt độ cao đến phản ứng hoàn toàn, thu được 8,96 lít hỗn hợp khí Y (đktc). Cho khí hấp thụ vào nước thu được 2 lít dung dịch Z và còn lại thoát ra 3,36 lít khí (đktc). pH của dung dịch Z là
A. pH = 0.
B. pH = 1.
C. pH = 2.
D. pH =3.
Tiến hành phản ứng nhiệt nhôm m gam hỗn hợp X gồm Al và Cr2O3 trong khí trơ, sau khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp chất rắn Y. Chia Y thành hai phần bằng nhau. Phần một phản ứng với dung dịch NaOH (loãng, dư), thu được 3,36 lít H2 (đktc). Phần hai phản ứng với dung dịch HCl (loãng, nóng, dư), thu được 12,32 lít H2 (đktc). Giá trị của m là: A. 74,3. B. 43,9. C. 57,4. D. 87,8.
Đọc tiếp
Tiến hành phản ứng nhiệt nhôm m gam hỗn hợp X gồm Al và Cr2O3 trong khí trơ, sau khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp chất rắn Y. Chia Y thành hai phần bằng nhau. Phần một phản ứng với dung dịch NaOH (loãng, dư), thu được 3,36 lít H2 (đktc). Phần hai phản ứng với dung dịch HCl (loãng, nóng, dư), thu được 12,32 lít H2 (đktc). Giá trị của m là:
A. 74,3.
B. 43,9.
C. 57,4.
D. 87,8.
Hoà tan hoàn toàn m gam bột nhôm trong dung dịch chứa HCl và HNO3 thu được 3,36 lít hỗn hợp Y gồm hai khí không màu, dung dịch còn lại chỉ chứa muối của cation Al3+. Đem toàn bộ lượng hỗn hợp khí Y trộn với 1 lít oxi thu được 3,688 lít hỗn hợp gồm 3 khí. Biết thể tích các khí đều đo ở đktc và khối lượng của hỗn hợp khí Y nhỏ hơn 2 gam. Tìm m. A. 9,72 gam. B. 8,10 gam. C. 3,24 gam. D. 4,05 gam.
Đọc tiếp
Hoà tan hoàn toàn m gam bột nhôm trong dung dịch chứa HCl và HNO3 thu được 3,36 lít hỗn hợp Y gồm hai khí không màu, dung dịch còn lại chỉ chứa muối của cation Al3+. Đem toàn bộ lượng hỗn hợp khí Y trộn với 1 lít oxi thu được 3,688 lít hỗn hợp gồm 3 khí. Biết thể tích các khí đều đo ở đktc và khối lượng của hỗn hợp khí Y nhỏ hơn 2 gam. Tìm m.
A. 9,72 gam.
B. 8,10 gam.
C. 3,24 gam.
D. 4,05 gam.
Hoà tan hoàn toàn m gam bột nhôm trong dung dịch chứa HCl và HNO3 thu được 3,36 lít hỗn hợp Y gồm hai khí không màu, dung dịch còn lại chỉ chứa muối của cation Al3+. Đem toàn bộ lượng hỗn hợp khí Y trộn với 1 lít oxi thu được 3,688 lít hỗn hợp gồm 3 khí. Biết thể tích các khí đều đo ở đktc và khối lượng của hỗn hợp khí Y nhỏ hơn 2 gam. Tìm m. A. 9,72 gam. B. 3,24 gam. C. 8,10 gam. D. 4,05 gam.
Đọc tiếp
Hoà tan hoàn toàn m gam bột nhôm trong dung dịch chứa HCl và HNO3 thu được 3,36 lít hỗn hợp Y gồm hai khí không màu, dung dịch còn lại chỉ chứa muối của cation Al3+. Đem toàn bộ lượng hỗn hợp khí Y trộn với 1 lít oxi thu được 3,688 lít hỗn hợp gồm 3 khí. Biết thể tích các khí đều đo ở đktc và khối lượng của hỗn hợp khí Y nhỏ hơn 2 gam. Tìm m.
A. 9,72 gam.
B. 3,24 gam.
C. 8,10 gam.
D. 4,05 gam.
Đáp án : B
nY = 0,15 mol giả sử gồm khí A và B
Vì VY + VO2 > V3 khí sau trộn => có phản ứng
=> Y có NO(A) : NO + ½ O2 à NO2
=> nO2 pứ = 1 + 3,36 – 3,688 = 0,672 ( < 1 lit ) ( O2 dư )
=> nNO = 0,06 mol => nB = 0,09 mol
Vì mY < 2 => MB < 18,3 => B là H2
Bảo toàn e : 3nAl = 2nH2 + 3nNO => nAl = 0,12 mol
=> m = 3,24g
Đúng 0
Bình luận (0)